Giant Virus / Pandoraviridae
パンドラウイルス
生命の定義を揺るがす「箱の怪物」
— THE PANDORA’S BOX OF LIFE SCIENCE —
顕微鏡の向こうに
現れた「異物」
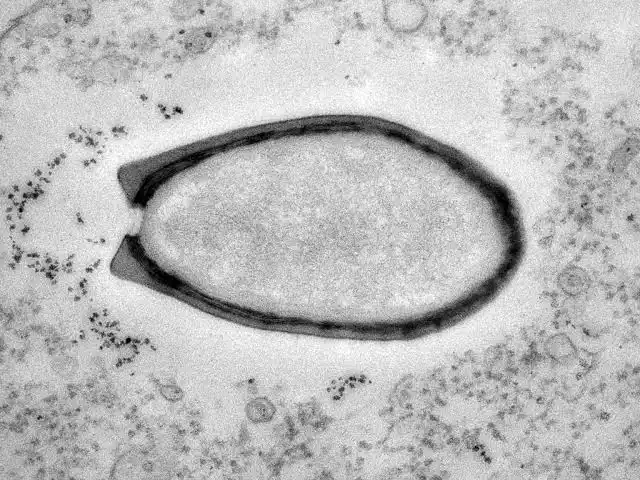
2008年、ドイツの寄生虫学者パトリック・シャイトは、角膜炎を患う女性の目から採取したアカントアメーバの中に、奇妙な構造体を発見した。それは、あまりにも大きすぎた——。
ドイツ連邦軍医療サービス中央研究所(コブレンツ)の寄生虫学者、パトリック・シャイト(Patrick Scheid)博士は、ルーティンワークのように顕微鏡を覗いていた。角膜炎の女性患者からコンタクトレンズを通して採取されたアカントアメーバ(Acanthamoeba)の培養サンプルを調べる、日常的な作業だった。しかし、その日の映像は、彼の経験のすべてに反するものだった。
アメーバの細胞内に、巨大な楕円形の構造体が潜んでいた。そのサイズは、通常のウイルスの10倍以上。いや、小さな細菌と比べても遜色ないほどの大きさだった。「ウイルスである」という発想は、シャイト博士の頭には最初から存在しなかった。あまりにも大きすぎたからだ。彼は慎重に記録を取り、この謎の生物を「内共生生物(endocytobiont)」と呼んで論文に記載した。しかし、それが何であるかは、ついに解明されなかった。
その「謎の構造体」が正体を明かすまでには、さらに5年の歳月が必要だった。2013年7月18日、科学誌『サイエンス(Science)』にひとつの論文が掲載された瞬間、世界中の微生物学者が息を呑んだ。フランス・エクス=マルセイユ大学の夫婦研究者、ジャン=ミシェル・クラブリー(Jean-Michel Claverie)教授とシャンタル・アベルジェル(Chantal Abergel)博士らが率いる研究チームが、まったく新しいタイプの巨大ウイルスを発見した。
その名前は、「パンドラウイルス(Pandoravirus)」。
ギリシャ神話の「パンドラの箱」から名付けられたその存在は、ウイルス学の常識を根底から覆しただけでなく、「生命とは何か」という哲学的問いにまで踏み込む、まさに「開けてしまった箱」となった。
「この発見は、私たちがウイルスだと思っていたものの土台を完全に壊してしまう。パンドラの箱を開けたのです」
ウイルスの常識、崩壊
「ウイルスは小さい」——この一文は、20世紀微生物学の鉄則だった。だがその鉄則は、気づかれることなく、長い間、すでに崩れていたのかもしれない。
科学の世界において、「常識」ほど危険なものはない。それは知識の積み重ねから生まれるものだが、同時に、まだ見ぬ真実への盲点にもなりうる。
20世紀の微生物学において、ウイルスに関するもっとも基本的な「常識」は次のようなものだった。ウイルスとは、光学顕微鏡では見えないほど小さい。遺伝子をほとんど持たず、非常にシンプルな存在だ。宿主の細胞を借りてしか増殖できず、自分自身では何もできない単純な「粒子」に過ぎない——。
この定義は、あながち間違いではない。HIVは約9個の遺伝子しか持たず、インフルエンザウイルスは8個、コロナウイルスでも約30個程度だ。サイズも25〜100ナノメートル程度で、光学顕微鏡の解像限界(約200ナノメートル)をはるかに下回る。こうした「典型的なウイルス」のイメージが、研究者の脳内に深く刻まれていた。
しかし——。
「ろ過性病原体」という呪縛
ウイルスはかつて「ろ過性病原体(filterable pathogen)」と呼ばれていた。孔径0.2マイクロメートルの滅菌フィルターを通過してしまう微粒子として定義されていたのだ。この定義は、1892年にドミトリー・イワノフスキーがタバコモザイク病の原因物質を発見したことに端を発し、以来100年以上にわたって微生物学の礎となってきた。しかしパンドラウイルスの粒子長は約1マイクロメートル——このフィルターを楽々と「通過できない」サイズだ。つまり、パンドラウイルスは定義の上でも「ウイルスではあり得ない」とみなされていたのである。
最初の「警告信号」は、2003年に発信されていた。フランスとイギリスの研究者たちが、英国ブラッドフォードの冷却塔の水から、異様に大きな粒子を持つウイルスを発見した。「ミミウイルス(Mimivirus)」と名付けられたそのウイルスは、約0.7マイクロメートルのサイズを持ち、1,000個以上の遺伝子を有していた。その名前は「microbe-mimicking virus(微生物を模したウイルス)」の略で、細菌のように振る舞うことへの驚きから付けられた。
ミミウイルスの発見は、確かにセンセーショナルだった。しかしその後、研究者たちはある程度「なるほど、ウイルスにもこういうものがいるのか」と消化しはじめていた。ミミウイルスが最大だろう、と多くの者が思っていた。
その「なるほど」が、2013年に粉砕された。
ゲノムサイズ比較 — ウイルスから細菌まで
では、なぜこれほど大きなウイルスが長い間見落とされてきたのか?その答えは、科学者たちの「思い込み」にある。パンドラウイルスを発見したクラブリーとアベルジェルは、この現象をこう説明する。「研究者が顕微鏡で細胞を観察するとき、通常のウイルスのサイズや形状からはずれているものを見ると、ウイルスだとは思わない。細菌の一種だろうと思う。そして細菌だと思って培養を試みると失敗する。でもそれも驚かない——海洋中の細菌の約60%は培養に失敗するのだから」
実際、ミミウイルス自体も最初の発見(1992年)から、ウイルスとして正式に認定されるまでに11年もかかっている。あまりに大きすぎたため、細菌として分類されていたのだ。パンドラウイルスの場合は、その「見落とし」がさらに徹底していた。発見チームが過去の文献を調査したところ、2000年に書かれたアカントアメーバの寄生生物に関する論文に、パンドラウイルスとよく似た「小片」の記載があったことが判明している。13年以上前から、その姿は目撃されていたのだ——誰もその正体を知らないまま。
「ウイルス(virus)」という言葉は、ラテン語で「毒(poison)」を意味する。生物としての定義は今も曖昧で、「自己複製能を持つが、細胞を持たず、独立した代謝を行わない存在」とされる。この定義をもとにすれば、ウイルスは「生きていない」ことになる。しかし、パンドラウイルスはこの境界線を笑うように踏み越えている。2,556もの遺伝子を持ち、宿主の核膜すら書き換え、独自のウイルス工場を細胞内に建設する——それは、もはや単なる「毒」ではなく、何か得体の知れない知的存在のように見える。
二つの「壺」、
地球の果てで目覚める
一方はチリの海岸、沖合の堆積物の中。もう一方はオーストラリア・メルボルン郊外の淡水池の底。15,000キロメートル離れた二か所で、ほぼ同時に巨人が眠りから覚めた。
パンドラウイルスの発見の物語は、二つの「場所」から始まる。
ひとつは、チリ中部の海岸線、トゥンケン川(Tunquen River)の河口付近。太平洋に注ぐこの川の沖合の堆積物から、クラブリー&アベルジェルの研究チームはサンプルを採取した。チリでのサンプリングが実現したのは、欧州の研究プログラム「ASSEMBLE(Association of European Marine Biological Laboratories)」のおかげだった。このプロジェクトは、ヨーロッパの研究者たちが世界各地の海洋研究施設を利用できる枠組みを提供しており、研究チームはそのネットワークを通じてチリ・ラス・クルセス(Las Cruces)の施設を利用した。
もうひとつは、オーストラリア・メルボルン郊外にあるラ・トローブ大学(La Trobe University)のキャンパス内の浅い淡水池。こちらは、研究者たちが「訪問した場所でランダムにサンプリングを行う」という習慣の産物だった。アベルジェル博士は後のインタビューで「オーストラリアのサンプルは、私たちが訪れた場所でたまたま行ったランダムなサンプリングの結果だ」と語っている。
これほど離れた二つの場所から、ほぼ同時に同じ種の巨大ウイルスが発見された——この事実は、研究チーム自身も驚かせた。「二つが同時に見つかったという事実は、私たちが信じられないほど運が良かったか、あるいはそれほどパンドラウイルスが稀ではないかのどちらかだ」とアベルジェルは述べている。
Pandoravirus salinus
「塩水のパンドラ」
Pandoravirus dulcis
「甘い水のパンドラ」
(2,473,870 塩基対)
(1,908,524 塩基対)
地球の正反対に近い
(幅 0.5 μm)
光学顕微鏡で見えるサイズ
両種のウイルスは、形が特徴的だ。「アンフォラ(amphora)」——古代ギリシャ・ローマで使われた、細長い壺の形——に酷似した楕円体の粒子を持つ。一端に「ostiole(気孔)」と呼ばれる開口部があり、ここからゲノムを宿主細胞に放出する。研究チームがパンドラウイルスを「パンドラの箱」と関連付けたのは、この壺型の形状と、そのゲノムから溢れ出る「未知の何か」への驚きの両方を込めてのことだった。
発見の手順は、こうだ。チームは採取した堆積物サンプルを、アカントアメーバ(Acanthamoeba spp.)の培養系に添加した。アカントアメーバは淡水・海水を問わず世界中に生息する原生生物で、多くの巨大ウイルスの宿主として知られている。もしサンプルにウイルスが潜んでいれば、アメーバへの感染と死亡(溶菌)が観察されるはずだ。
実際、アメーバは死に始めた。そして電子顕微鏡でその死骸を調べると——前代未聞の粒子が見えた。
「通常、顕微鏡でウイルスを見ると結晶のように見える。しかしパンドラウイルスは、細胞構造のように見えた。最初は特別な細菌かもしれないと思った。その大きさと形態のせいで。しかし、さらなる検査でウイルスだと確認された」
電子顕微鏡による観察と感染サイクルの追跡調査が始まった。パンドラウイルスがアカントアメーバに感染する過程は、既知のウイルスとは根本的に異なる異様さを帯びていた。
まず、ウイルス粒子がアメーバの膜小胞(ファゴソーム)との融合によって細胞内に侵入する。侵入したパンドラウイルスは、そのまま静かに細胞の「奥」へと向かう。そして——ここが最も驚くべき点だが——宿主の核膜を破壊し、核の中身を完全に書き換え始めるのだ。核膜の形状が変容し、内容物が再構成される。感染から8〜10時間後には、宿主細胞が球形に縮み始め、新しいウイルス粒子が細胞内に生成されているのが確認される。やがて細胞は崩壊し、新世代のパンドラウイルスが放出される。
この「核の乗っ取り」は、ミミウイルスとも根本的に異なる戦略だ。ミミウイルスは細胞質内に独立した「ウイルス工場」を作るのに対し、パンドラウイルスは宿主の核そのものを工場に変えてしまう。まるで会社を乗っ取るのではなく、本社ビルを丸ごと改造するような所業だ。
パンドラウイルスの感染サイクル詳細
①ウイルス粒子がアカントアメーバに認識され、食作用(phagocytosis)によって細胞内に取り込まれる。②液胞(vacuole)内で頂端の開口部(ostiole)が開き、ゲノムDNAが細胞質へと放出される。③ゲノムが宿主の核へと移動し、「蝕食相(eclipse phase)」が始まる(約2〜4時間)。④宿主の核膜が変形・崩壊し始め、核内が再編成される。この段階での核の構造変化は、パンドラウイルス固有の特徴である。⑤感染8〜10時間後、新しいウイルス粒子が細胞内で組み立てられる。⑥感染12〜15時間後、細胞が崩壊(溶菌)し、新世代ウイルス粒子が放出される。一部は細胞外排出(exocytosis)によっても放出される。
さらに奇妙なのが、その「組み立て方」だ。通常のウイルスは、まず空のカプシド(殻)を作り、その後でゲノムDNAを内部に詰め込む、という2段階のプロセスを踏む。しかしパンドラウイルスでは、殻の構築とDNAの充填が同時並行で進む。クラブリーとアベルジェルはこのプロセスを「ニッティング(knitting)」と名付けた——編み物のように、一つ一つ織りながら形が生まれていく様子から。
このニッティングのプロセスは、真核生物の細胞核形成を彷彿とさせるとも指摘されている。細胞核もまた、DNA複製と核膜形成が密接に絡み合いながら組み立てられるからだ。パンドラウイルスの振る舞いが、ウイルスよりも細胞のそれに似ているという印象を与えるのは、こうした点からも理解できる。
パンドラウイルスの粒子形状が「アンフォラ(古代の壺)」に似ていることは、命名の際に重要な根拠となった。しかしこれは単なる形状の比喩以上の意味を持つ。ギリシャ神話において、パンドラが解き放った「箱(ピトス)」は、実は壺型の容器だった。後世に「箱(box)」と誤訳されることが多いが、本来は大型の甕(かめ)型容器「ピトス(pithos)」だ。パンドラウイルスの後に発見された別の巨大ウイルス「ピトウイルス(Pithovirus)」は、まさにこの「ピトス」から名を取っている。つまり「パンドラウイルス」と「ピトウイルス」は、神話の中で同じ壺をめぐる、2種の巨人の兄弟のような関係にある。形状も似ているが、ゲノムサイズは大きく異なる——パンドラウイルスが巨大なゲノムを持つのに対し、ピトウイルスはより大きな粒子を持ちつつゲノムはずっと小さいという「逆転現象」も興味深い。
夫婦科学者の
情熱と執念
パンドラウイルスの発見は、偶然ではなかった。それは、「限界があるはずのない」という信念を持ち続けた二人の科学者が、何年もかけて積み上げた執念の産物だった。
エクス=マルセイユ大学教授、フランス国立科学研究センター(CNRS)研究員。ゲノム情報科学と巨大ウイルス研究の第一人者。ミミウイルス研究にも関与し、「ウイルスの宇宙の限界は存在しない」という持論を長年唱え続けてきた。科学者として珍しく、発見の「熱狂」を率直に表現することで知られる。「50年に一度の発見だ」という言葉は、世界中のメディアに引用された。
エクス=マルセイユ大学の研究所(IGS: Structural and Genomic Information Laboratory)のディレクター・オブ・リサーチ。クラブリーの妻であり、研究上のパートナーでもある。ミミウイルス、メガウイルスに続くパンドラウイルスの発見を主導。巨大ウイルスが地球規模で分布していることを確認し、「15,000km離れた二か所での同時発見は、パンドラウイルスが珍しくないことを示している」と語った。科学者でありながら、常に社会への影響と問いかけを意識した発言でも注目される。
クラブリーとアベルジェルが巨大ウイルスの研究に情熱を注ぐようになったのは、2003年のミミウイルス発見がきっかけだった。イギリスとフランスの共同チームが英国ブラッドフォードの冷却塔の水から発見したミミウイルスは、当時の常識を覆す0.7マイクロメートルの巨大ウイルスだったが、クラブリーとアベルジェルはその意義をいち早く理解した。「ウイルスのサイズと複雑さには上限がない」という命題が、彼らの研究テーマの中心に据えられた。
2009年にはミミウイルスとそのウイルスファージ(ウイルスに感染するウイルス)に関するレビュー論文を発表し、2011年にはメガウイルス・キレンシスの発見に貢献した。そして2013年のパンドラウイルス発見に至るまで、彼らはチリや世界各地の海洋・淡水堆積物から積極的にサンプリングを続けていた。
パンドラウイルスを発見した際、アベルジェル博士は「私たちは巨大ウイルスが1,000の遺伝子を持つことを想定していた。しかし発見した一方のウイルスは2,556の遺伝子を持っていた。それは巨大だった」と振り返っている。発見者でさえ、その大きさに驚かされたのだ。
夫婦での共同研究というスタイルは、研究の継続性と深さを生んでいる。二人は同じ研究室(IGS: Institut de Génomique Structurale et Fonctionnelle)に所属し、ミミウイルス研究から巨大ウイルス全般へと研究を広げてきた。後年のピトウイルス(3万年前の永久凍土から復活)や、2022年の「ゾンビウイルス」研究においても、彼らのコンビネーションが威力を発揮している。
IGS研究室の巨大ウイルス発見年表
クラブリー&アベルジェルらのエクス=マルセイユ大学・IGS研究室は、現代の巨大ウイルス研究をリードしてきた:
2003年:ミミウイルス(Mimivirus)の正式認定に貢献。1992年発見だが、2003年まで細菌と誤認されていた。
2011年:メガウイルス・キレンシス(Megavirus chilensis)発見。チリ沖から採取。当時最大のウイルス。
2013年:パンドラウイルス(Pandoravirus)発見。2種。Science誌掲載。世界に衝撃。
2014年:ピトウイルス・シベリクム(Pithovirus sibericum)発見。3万年前の永久凍土から復活に成功。
2015年:モリウイルス・シベリクム(Mollivirus sibericum)発見。同じ凍土サンプルから。
2018年:パンドラウイルス3新株の発見とde novo遺伝子創造機構の解明(Nature Communications)。
2022年:シベリア永久凍土から13種の新巨大ウイルスを復活。最古は48,500年前(Viruses誌)。
論文の筆頭著者はナデージュ・フィリップ(Nadège Philippe)とマチュー・ルジャンドル(Matthieu Legendre)ら若手研究者だったが、研究室の指導者として、そして巨大ウイルスへの長年の情熱を持つ科学者として、クラブリーとアベルジェルは本発見の実質的な立役者だ。論文の発表後、世界中のメディアが二人へのインタビューを求めた。
アベルジェルはFrance24のインタビューで、こう語った。「この発見はパンドラの箱を開けた。私たちがウイルスだと思っていたものの認識を根本から変えることになるだろう。パンドラウイルスは非常に複雑だ。遺伝子の90%は未知のものだ。これは進化生物学に対する私たちの認識を再考させることになる」
クラブリーはナショナルジオグラフィックのインタビューで「こんなに異なる新タイプのウイルスを見つけることは、50年に一度ある——主要な発見だ」と述べた。この言葉は、誇張ではなかった。
93%が「未知」という
衝撃のゲノム
パンドラウイルス・サリヌスの遺伝子2,556個を解析した結果、研究者たちは血の気が引く数字を目にした。そのうち93%が、地球上のいかなる既知の生物のいかなる既知の遺伝子とも——一切の関連を持たないのだ。
ゲノム解析の結果が出た瞬間、研究チームは静まり返ったという。
現代の生物情報学では、ゲノムを解析すると、その遺伝子がどんな生物に似ているか、どんな機能を持つかが「データベースとの照合」によって即座にわかる。NCBI(米国国立生物技術情報センター)が管理するGenBankをはじめ、世界中の生物のゲノムデータが格納された巨大なデータベースに照合することで、未知の生物の遺伝子でも「これはあの酵素に似ている」「あの生物の祖先と関係がありそう」といった推定ができる。
しかしパンドラウイルスのゲノムは、違った。
2,556個の遺伝子のうち、既知のデータベースで「対応する機能が判明している」ものは7%以下。残りの93%以上は、地球上のいかなる生物のいかなる遺伝子とも、有意な類似性を示さなかった。つまり、その遺伝子たちが何をしているのか、何から進化したのか——まったくわからないのだ。
対応なしの遺伝子割合
(P. salinus)
既知の遺伝子割合
既知の機能を持つもの
(発見当初の推定)
(タンパク質翻訳機能なし)
比較として:ヒトゲノムは約24,000個の遺伝子を持ち、その大部分は他の動物、さらには細菌との遠い共通祖先を持つ遺伝子として追跡できる。大腸菌(Escherichia coli)でさえ、その約4,400個の遺伝子の多くは他の細菌との共通の歴史を持つ。進化の木をどれだけ遡っても、ほとんどの生物は「共通の遺産」を持っている。なぜなら、すべての地球上の生物は共通祖先(LUCA: Last Universal Common Ancestor)に由来すると考えられているからだ。
しかしパンドラウイルスの遺伝子の93%は、その系統樹のどこにも位置づけられない。LUCA以前に分岐したか、あるいはLUCAとは全く別の起源を持つか——どちらであれ、それは地球の生命史の根幹を揺るがす発見だった。
この「未知の93%」をどう解釈するかをめぐって、科学者の間で大きな議論が生まれた。大きく分けると、三つの仮説が浮かびあがる。
「第四のドメイン」仮説——未知の生命系統への帰属
クラブリーとアベルジェルを含む一部の研究者が支持する仮説。パンドラウイルスの遺伝子群が既知の生物と無関係なのは、パンドラウイルスが「細菌・古細菌・真核生物」の三ドメインとは別の、第四の系統に属する生命体の子孫だからではないか——という考え。これは、かつて生命の世界に「第四の枝」が存在し、現在のパンドラウイルスとその近縁ウイルスがその生き残りである可能性を示唆する。論文中でも「第四のドメインの存在という議論の余地ある仮説を支持する」と記載されている。
「縮退した細胞生物」仮説——かつて生きていた生物の成れの果て
パンドラウイルスは、かつて独立して生きていた細胞生物が、長い進化の過程でウイルスへと「縮退(退化)」したものではないか、という仮説。細菌の中にも、宿主細胞への寄生に特化して自らの代謝機能を次々に失ったもの(例:マイコプラズマ)がいる。パンドラウイルスは、この「縮退」がさらに極端に進んだ結果、リボソームや一部の代謝遺伝子を捨てつつも、膨大な「未知の遺伝子」を保持した状態になったのかもしれない。
「デノボ遺伝子創造」仮説——無から遺伝子を生み出す工場
2018年のNature Communications論文で有力になった仮説。パンドラウイルスの「孤児遺伝子(ORFan)」は、他の生物から盗んだものでも、既存の遺伝子が変異したものでもなく、de novo(新たに)、ゲノムの非コード領域(本来は遺伝子として機能しない部分)から自発的に生み出されたものではないか——という考え。つまりパンドラウイルスは、まるで「遺伝子の製造工場」のように、無から新しい遺伝子を生み出し続けている可能性がある。
2018年の研究では、マルセイユ(フランス本土)、ヌーメア(ニューカレドニア)、メルボルン(オーストラリア)で新たに採取された3株のパンドラウイルスと、ドイツで発見された1株、合計6株のゲノムを比較解析した。その結果、興味深い事実が明らかになった。
まず、形状や機能が酷似しているにもかかわらず、6株がタンパク質コード遺伝子を共有しているのはわずか半分程度だった。通常、同じ「ファミリー」に属するウイルスなら、もっと多くの遺伝子を共有するはずだ。さらに、各株に固有の「孤児遺伝子」が大量に存在しており、これらの遺伝子は統計的性質が「ゲノムの非コード領域に由来する」ことと一致していた。
CNRS(フランス国立科学研究センター)は2018年6月のプレスリリースでこう述べた:「パンドラウイルスは自分の遺伝子を発明している。自然界の”モンスター”から進化の革新者へ——巨大ウイルスは生命の樹に衝撃を与え続けている」
「この謎めいた特性は、ウイルスの起源をめぐる多くの議論の核心にある。パンドラウイルスは、遺伝子の工場のようだ——新しい遺伝子を、そして新しい機能を次々と作り出している」
さらに驚くべき発見が続く。2019年以降の研究では、パンドラウイルスのゲノムに「AGCT」という特定の4塩基配列(テトラヌクレオチド)が、一部の株でほぼ完全に欠如していることが発見された。この特定配列の欠如は、パンドラウイルス以外のいかなる生物でも確認されておらず、「他のどの微生物にも見られない、未解明の進化プロセスの産物」と解釈された。
パンドラウイルスのゲノムは、まるで人類がまだ文字を持っていない言語で書かれた古文書のようだ。何かが書かれているのはわかる。それが巨大で複雑であることもわかる。しかし、その内容は——いまだ、ほとんど読めない。
パンドラウイルスの宿主であるアカントアメーバ(Acanthamoeba)は、それ自体が非常に興味深い生物だ。土壌、海水、淡水、さらには病院の水道管や空調システムにまで広く生息し、ヒトの角膜炎(アカントアメーバ角膜炎)や脳炎(肉芽腫性アメーバ性脳炎)の原因になることもある。アカントアメーバはコンタクトレンズ使用者の目の中でも生育でき、2008年のシャイト博士の発見もそこから生まれた。同時に、アカントアメーバは他の微生物を貪食する「ゴミ収集車」のような存在でもあり、巨大ウイルスを含む多種多様なウイルスの「避難所」「培養基」として機能している可能性がある。巨大ウイルスが多様に進化できたのは、この「何でも飲み込むアメーバ」という安定した宿主の存在があったからかもしれない。
第四のドメインを巡る
大論争
「細菌・古細菌・真核生物」——現代生物学が認める生命の3つの「ドメイン(領域)」。パンドラウイルスの発見は、そこに第四の柱を打ち立てる可能性を示した。世界の生物学者たちは、賛成と反対に真っ二つに割れた。
現代の生物学において、地球上のすべての生命は三つの「ドメイン(超界)」に分類されると考えられている。カール・ウーズ(Carl Woese)とジョージ・フォックス(George Fox)が1977年に16S rRNAの系統解析をもとに提唱した「三ドメイン説」だ。
第一のドメインは「バクテリア(Bacteria / 細菌)」。大腸菌や乳酸菌など、核膜を持たない原核生物。第二は「アーキア(Archaea / 古細菌)」。熱水噴出孔や塩湖など極端な環境に生きる原核生物で、細菌とは独立した系統を持つ。第三が「ユーカリア(Eukarya / 真核生物)」。核膜を持つ細胞からなる生物で、アメーバから人間まで含む。
ウイルスは、この三ドメインのいずれにも属さない。独自の細胞を持たず、独立した代謝を行わず、宿主なしには存在できないため、「生物ではない」とみなす立場が長く支配的だった。
しかしパンドラウイルスの発見は、この構図を根本から揺るがした。
生命の分類体系と、ウイルスの「除外」
カール・ウーズとジョージ・フォックスが提唱した三ドメイン説は、リボソームRNA(rRNA)の塩基配列分析に基づく。すべての生物は翻訳機構(リボソーム)を持つため、rRNAは普遍的な「生命の指紋」となる。しかしウイルスはリボソームを持たないため、この分析ができない。これがウイルスを「生命の系統樹の外」に置く一因となってきた。パンドラウイルスもリボソームを持たないが、2,556個の遺伝子という複雑さは、リボソームを持つ一部の細菌(マイコプラズマ、ナノアルカエウム)よりも圧倒的に大きい。「リボソームを持たない=生物でない」という論理が、パンドラウイルスの前では説得力を失いつつある。
パンドラウイルスの論文の中でクラブリーとアベルジェルが示した、もっとも大胆な主張はこうだ。
「パンドラウイルスのDNAポリメラーゼは、他の巨大DNAウイルスのものとクラスタリングする。これは、議論の余地はあるが、第四のドメインの存在を示唆する可能性がある」
この「議論の余地がある(controversial)」という留保を付けながらも第四のドメインの可能性に言及した一文は、世界の生物学コミュニティに激震をもたらした。
「三ドメイン説は『おそらくかなり間違っている』——私たちはパズルの欠けたピースを見逃している」
「第四のドメイン仮説」の支持者たちは、主に次の論拠を挙げる。
まず、パンドラウイルスの遺伝子93%が既知のいかなる生命体とも無関係という事実。もし巨大ウイルスが既存の生物(細菌、古細菌、真核生物)から進化したなら、もっと多くの「共通遺産」が残っているはずだ。共通遺産がほとんどないということは、パンドラウイルスの系統が既知の三ドメインから非常に早期に——おそらく数十億年前に——分岐したことを意味する可能性がある。
次に、DNAポリメラーゼ(DNA複製を担う酵素)の系統解析。パンドラウイルスのDNAポリメラーゼは、ミミウイルスなど他の巨大DNAウイルスのものと近縁であり、細菌・古細菌・真核生物のいずれのポリメラーゼとも異なる独自のクレードを形成している。これは、巨大ウイルス全体が共通の「第四の系統」に属する可能性を示唆する。
しかし、世界中の多くの著名な科学者がこの「第四のドメイン説」に強く反論している。フランスのパトリック・フォルテール(Patrick Forterre)、マルト・クルポヴィッチ(Mart Krupovic)、ダヴィット・プランギシュヴィリ(David Prangishvili)らは2014年に、『Trends in Microbiology』誌上で反論論文を発表した。彼らの主な論点は以下の通りだ。
①ウイルスは細胞分裂ではなく感染増殖によって増えるため、三ドメインの系統樹と同じ枠組みで比較することは根本的に不適切である。
②大型ウイルスは「ここにも、あそこにも、いたるところで」独立して進化してきた可能性が高く、すべてをひとつの「第四のドメイン」に押し込めることは進化生物学を複雑にするだけだ。
③RNAポリメラーゼを使って生命の樹を描き直すことは巨大な困難を伴う——大型ウイルスはひとつの新ドメインに集約されない。
④パンドラウイルスの「孤児遺伝子」93%は、第四のドメインの証拠ではなく、de novo遺伝子創造や水平遺伝子転移などの通常の進化メカニズムで説明できる可能性がある。
カナダ・ブリティッシュコロンビア大学のウイルス学者カーティス・サトル(Curtis Suttle)はNature誌のコメントで、「ウイルスを第四のドメインとして考えることは、科学的合理性の限界を超えている」と述べた。一方でレアル・クリアサイエンス(RealClearScience)は「第四のドメイン説は科学界で論争中であり、性急な結論は禁物だ」と報じた。
この論争は現在も決着がついていない。それどころか、新しい発見のたびに新しい議論が生まれ、「生命とは何か」という根本問題への関心を絶えず掻き立て続けている。
特に注目されているのが、「細胞核のウイルス起源説」だ。東京理科大学の武村政春教授が2001年に提唱したこの仮説では、大型DNAウイルスの祖先が古細菌に感染・共生することで真核生物の細胞核が形成されたと考える。もしこれが正しければ、動植物を含むすべての真核生物の細胞核は——ウイルスに由来することになる。パンドラウイルスの「核を乗っ取る」振る舞いは、その「原始的な記憶」の再現のように見えなくもない。
パンドラウイルスの発見は、「生命の定義」という哲学的問いを改めて突きつけた。現在、最も広く使われる「生命」の定義は「①自己複製できる、②代謝を行う、③外界と膜で仕切られた区画を持つ」というものだ。ウイルスは③と②を欠くためこの定義では「非生命」とされる。しかしパンドラウイルスは、宿主の核を乗っ取って自らの「工場」を作り、2,556の遺伝子を動員して複雑な構造体を組み上げる。これを「非生命の機械的な複製」と呼ぶことは、あまりにも素朴な見方ではないか? 少なくとも、ウイルスを「生きていない」と簡単に片付けてきた従来の定義は、パンドラウイルスの存在によって深刻な問い直しを迫られている。一部の研究者は、ウイルスを含む新たな「生命のスペクトラム」という概念を提唱し始めている。
自分で遺伝子を発明する
——無からの創造
進化論の教科書は、遺伝子は「変異」「複製ミス」「水平移動」によって変化すると教える。しかしパンドラウイルスは、それを超えた何かをやっているかもしれない——「無(非コード配列)から、新しい遺伝子を創り出す」という、前代未聞のメカニズムを。
2018年6月11日、Nature Communications誌に掲載された論文「Diversity and evolution of the emerging Pandoraviridae family」は、パンドラウイルス研究に新たな驚きをもたらした。著者はマチュー・ルジャンドル(Matthieu Legendre)、エリザベート・ファーブル(Elisabeth Fabre)、オリビエ・ポワロ(Olivier Poirot)、サンドラ・ジューディ(Sandra Jeudy)らを中心とする、CNRS・エクス=マルセイユ大学のチームだ。
研究チームは、以前の2株(サリヌスとドゥルキス)に加え、フランス・マルセイユ(P. quercus)、ニューカレドニア・ヌーメア(P. neocaledonia)、オーストラリア・メルボルン(新株)で発見した3株と、ドイツで発見された1株の計6株のパンドラウイルスゲノムを徹底的に比較解析した。転写物解析(トランスクリプトーム)、タンパク質解析(プロテオーム)、バイオインフォマティクス解析を組み合わせた、当時最も包括的なパンドラウイルス研究だった。
6株比較解析で明らかになった衝撃の事実
発見①:6株のパンドラウイルスは形態・機能が酷似しているにもかかわらず、タンパク質コード遺伝子を共有しているのは約50%程度。通常、同ファミリーのウイルスはもっと多くを共有する。
発見②:各株に固有の「孤児遺伝子(ORFan)」が大量に存在し、これらは既知のいかなる生物のゲノムにも相当するものがない。
発見③:孤児遺伝子のG+C含量、ORF長、CAI値(コドン適応指数)などの統計的性質が、「コアゲノム遺伝子」と「ゲノムの非コード領域(イントロン的領域)」の中間に位置する——これは、孤児遺伝子が「非コード領域から徐々に遺伝子として機能し始めた」過程を示唆する。
結論:パンドラウイルスのゲノムは「開いたパンゲノム(open pan-genome)」を持つ。遺伝子の重複や水平移動では説明できないほど多くの固有遺伝子が存在し、de novo遺伝子創造(非コード配列からの新遺伝子創生)が起きていると推定される。
「de novo遺伝子創造」とは何か?
遺伝子の進化には、従来いくつかの標準的なメカニズムが知られている。既存遺伝子の「複製と変異」、別の生物からの「水平遺伝子転移(HGT)」、遺伝子の「重複と機能分化」——これらがオーソドックスな説明だ。しかしde novo遺伝子創造は、これとは根本的に異なる。
ゲノムのほとんどの部分は「非コード領域」であり、タンパク質をコードしない。人間のゲノムでいえば、コーディング配列は全体の約2%に過ぎず、残りは「ジャンクDNA」と長らく呼ばれてきた(現在はこの名称は不適切とされている)。de novo遺伝子創造とは、この「ジャンク」的な非コード配列が、偶然の変異の積み重ねによって「機能を持つタンパク質をコードする遺伝子」へと変化するプロセスだ。
これは、たとえるなら——意味のない文字の羅列が、偶然に「小説の一節」として機能し始めるようなものだ。確率論的には起こりにくい。しかしパンドラウイルスのゲノムでは、それが繰り返し起きているように見える。なぜか?
パンドラウイルスのゲノムは2.5メガ塩基という巨大さを誇り、その非コード領域も膨大だ。感染サイクルが高速で(1サイクル約12〜15時間)、宿主(アカントアメーバ)が豊富な水環境に広く生息するため、大量の複製機会がある。これらの条件が重なることで、非コード配列が遺伝子へと「昇格」する確率が上がり、機能を獲得した新遺伝子が保持されやすくなっているのかもしれない。
「この孤児遺伝子たちが、段階的な進化の中間段階を経てどのように選択的機能を獲得したかは、いまだ謎の部分だ。de novo遺伝子創造のシナリオのダークな部分がそこにある」
さらに、2019年のバイオアーカイブ(bioRxiv)にアップされた論文では、パンドラウイルスのゲノムから「AGCT」という4塩基配列が特定の株において完全に消失していることが報告された。カオスゲーム表現(Chaos Game Representation)という手法でゲノム全体の塩基組成を視覚化したところ、この「AGCT」が一部株ではほぼゼロであることが判明したのだ。
この特定4塩基配列の欠如は、他のいかなる生物・ウイルスでも確認されていない。研究者たちは「いかなる他の微生物でも見られない、未解明の進化的選択プロセスの結果」と説明したが、そのプロセスが何であるかは、まだ解明されていない。
パンドラウイルスは、既存の生命の論理では説明できない方法で進化し、既存の生物語彙にない遺伝子を書き続けている。それは、地球上の生命の歴史において、私たちが読んでいない「別の章」の存在を示唆する。
2023年に発表された研究(「Evolution of giant pandoravirus revealed by CRISPR/Cas9」)では、ゲノム編集ツールCRISPR/Cas9を使ってパンドラウイルスと宿主のアカントアメーバの両方を遺伝子操作することに初めて成功した。この研究では、パンドラウイルスが小型の正二十面体ウイルスから「段階的な進化」によって壺型の巨大ウイルスへと変化したことを示す証拠が提示された。正二十面体の主要カプシドタンパク質の遺伝子を不活性化すると、ウイルスの形状が変化するという実験結果も得られた。CRISPR/Cas9によって「パンドラウイルスをハックする」ことが可能になったことは、今後の巨大ウイルス研究に革命をもたらす可能性を秘めている。ウイルスの機能ゲノミクスという、長らく手つかずだった分野への扉が開いた瞬間だ。
永久凍土に眠るゾンビたち
——温暖化が開ける「別の箱」
シベリアの大地の下、3万年前から眠り続けていた巨大ウイルスが、研究室で復活した。そして2022年、48,500年前のウイルスが再び息を吹き返した。気候変動が永久凍土を融かすとき、古代の「箱」は次々に開いていく。
2014年3月、クラブリーとアベルジェルのチームが学術誌『PNAS(米国科学アカデミー紀要)』に発表した論文は、パンドラウイルスの発見に劣らぬ衝撃を科学界に与えた。
彼らは、2000年に採取されていたシベリア北東部の永久凍土の土壌コア——地表下約30メートル(100フィート)の地点から——を実験室でアカントアメーバに晒した。すると、アメーバが感染死し始めた。凍土の中に、今なお感染能力を持つウイルスが生きていたのだ。
発見されたウイルスは「ピトウイルス・シベリクム(Pithovirus sibericum)」と命名された。放射性炭素年代測定による推定年齢は30,000年以上。後期更新世(プライストシーン)の時代、ネアンデルタール人がまだ地球上を歩き回っていた頃のウイルスが、3万年の眠りから覚めたのだ。
ピトウイルスはパンドラウイルスと同じ「壺型」の粒子形状を持つが、ゲノムサイズはわずか約600キロ塩基対——パンドラウイルスの4分の1以下だ。ただし粒子サイズはパンドラウイルスより50%大きく(長さ1.5μm)、粒子の大きさとゲノムの複雑さが必ずしも一致しないことを示している。
推定年齢(年)
復活後も感染能力を保持
最大推定年齢(年)
史上最古の復活ウイルス
復活した新ウイルス数
(5つの異なるファミリー)
地下深度
(地表から100フィート)
なぜ凍土の中でウイルスが「生き続ける」のか?
クラブリーとアベルジェルは、シベリア北東部の永久凍土の特性に注目する。「中性のpH、還元的環境(酸素が少ない)、嫌気的条件、暗黒——これらの条件が組み合わさることで、永久凍土はDNAを非常に長期間保存できる。凍土はタイムカプセルとして機能している」。巨大ウイルスはまた「開けるのが非常に難しい——通常のウイルスに比べて、物理的・化学的処理に対して極めて頑健だ」と彼らは指摘する。
2015年には同じ凍土サンプルから、さらに別のタイプの巨大ウイルス「モリウイルス・シベリクム(Mollivirus sibericum)」が発見された。モリウイルスは球形の粒子(直径0.6μm)を持ち、約651キロ塩基対のゲノムを有する。一つの凍土サンプルから複数の巨大ウイルスが発見されたことで、永久凍土が「巨大ウイルスの宝庫」であることが確認された。
そして2022年、クラブリー&アベルジェルのチームは決定的な論文を発表した(bioRxiv → Viruses誌掲載)。シベリアのさまざまな場所から採取した7種の永久凍土サンプルと、さらにレナ川(Lena River)とカムチャッカ(Kamchatka)の凍土から採取したサンプルから、合計13種の新しい巨大ウイルスを復活させることに成功したのだ。
これらは5つの異なるウイルスファミリーに属し、パンドラウイルスを含む——つまり、パンドラウイルスも永久凍土に保存されていたことが確認された。発見されたウイルスの年代は、凍土の放射性炭素年代測定によって推定され、最古のものは48,500年前にさかのぼる。このサンプルは、シベリアの地下湖から採取されたものだった。
「もし生きているウイルス粒子がまだそこにあるなら、それは大惨事へのレシピだ。採掘や掘削は、これらの古い層を何百万年ぶりに掘り起こすことを意味する」
クラブリー教授は特に、天然痘(smallpox)ウイルスの復活リスクについて警告している。「もしこれらのウイルス(アメーバを感染させる巨大ウイルス)が同じように生存するなら、天然痘は地球から根絶されていない——表面からだけ」と彼は述べる。「地下深くに掘り進めば、天然痘が再び人類の病気になる可能性を再び開く可能性がある」
この警告は現実の問題だ。2016年8月、ロシア北部で12歳の少年が死亡し、約20人が入院した。原因は炭疽菌(anthrax)——75年以上前に死んだトナカイの死体が、シベリアの夏の異常高温(35℃)によって融解した凍土から掘り出され、炭疽菌が放出されたのだ。天然痘ではなかったが、「凍土が病原体を封じ込めていた蓋になっていた」という構図は完全に現実化した。
永久凍土融解と病原体リスク——現状と見通し
永久凍土の現状:北半球の陸地面積の約22%(約2,300万平方km)が永久凍土に覆われている。シベリア、カナダ北部、アラスカなどが主な分布域。
融解の進行:気候変動により、北極圏の気温上昇は世界平均の2〜4倍速い。2050年までに永久凍土の30〜40%が消失する可能性があると一部の研究者は推測している。
既知の脅威:炭疽菌(2016年にシベリアで実例)、1918年スペイン風邪ウイルス(フラッド島の凍土に保存されている可能性)、各種人獣共通感染症ウイルスの保存。
巨大ウイルスについての楽観論:バンクーバー大学のカーティス・サトル博士はこう述べている:「人々はすでに毎日数千のウイルスを吸い込み、海で泳ぐたびに数十億のウイルスを飲み込んでいる。凍土が融けたウイルスが人類の健康に大規模に影響を与えるという考えは、科学的合理性の限界を超えている」
懸念される要素:クラブリーらの2022年の研究は、「アメーバを感染させるウイルスが長期保存後も感染能力を維持しているという事実は、他の多種多様なウイルス——アカントアメーバ以外の宿主を感染させるものも含め——が同様の条件下で感染能力を保持している可能性を合理的に示唆する」と結論付けている。
この論争において、多くの専門家は現在のところ「巨大ウイルス自体は人間に直接的な脅威を与えない」という立場を取っている。パンドラウイルスやピトウイルスはアカントアメーバを感染させるのみで、人間の細胞には感染しない。しかしクラブリーらは、これらの研究が「代理指標(surrogate)」として機能すると主張する。巨大ウイルスが復活できるなら、まだ人間に感染力を持つ古代の病原体も保存されているかもしれない——という警告だ。
地球温暖化と化石燃料採掘、さらには北極圏への観光・開発の進行は、この「パンドラの凍土」を日々少しずつ開けている。
クラブリーらが凍土からウイルス探索を始めたきっかけのひとつは、2012年に発表された別の研究だった。ロシアの科学者たちが、シベリアの永久凍土から採取した30,000年前のシレネ・ステノフィラ(Silene stenophylla)という植物の果実組織から、生きた植物を再生させることに成功したのだ。「植物の果実が3万年後に発芽できるなら、ウイルスも生き残れるのではないか」——この発想の飛躍が、ピトウイルスとパンドラウイルスの凍土からの復活へとつながった。科学的な発想の転換がいかに重要かを示す、美しい連鎖だ。ちなみにシレネ・ステノフィラの再生実験は、30,000年前の生物を生き返らせた史上初の成功例として記録されている。
海洋生態系の
影の支配者
パンドラウイルスは人間に害を与えないが、地球に害を与えていないわけではない——いや、むしろ逆だ。彼らは地球の酸素の半分を管理する「見えない調整者」として、海洋生態系の根底を支えているかもしれない。
パンドラウイルスは「人間には感染しない」と繰り返し強調される。しかし、これは「無害だ」という意味ではない。微生物の世界では、もっとスケールの大きな「影響力」が問題になるのだ。
海洋ウイルスは、地球規模の生態系に計り知れない影響を与えている。海洋中には1リットルあたり約1,000億個のウイルス粒子が存在し、毎日地球規模で約1,000兆個(10²³個)のウイルス感染が起きていると推定されている。この感染の多くが植物プランクトン(フィトプランクトン)を標的としており、フィトプランクトンの個体群を調節している。
フィトプランクトンは地球の酸素供給の約50%を担い、海洋食物連鎖の最底辺を支える存在だ。フィトプランクトンが増えすぎれば特定の種が支配的になり生態系の多様性が失われる。しかしウイルスがその個体群を選択的に「刈り取る(lysis)」ことで、多様性が維持されている。この調節機能を「ウイルスシャント(viral shunt)」と呼び、炭素循環や窒素循環にも深く関わっている。
ウイルスシャント——海洋生態系の隠れた調節システム
海洋中のウイルスによる感染・溶菌は、毎日海洋バイオマスの約20〜40%を分解すると推定されている。溶菌された微生物の細胞内容物(有機物・炭素・栄養塩)は「ウイルスシャント」を通じて、次の段階の食物連鎖(動物プランクトンなど)に直接移行するのではなく、溶存有機物(DOM)として水中に放出される。これが細菌による分解を経て、炭素・窒素・リンを海洋の化学サイクルに還元する。
パンドラウイルスのような巨大ウイルスが、この「ウイルスシャント」でどの程度の役割を担っているかは未解明だ。しかしパンドラウイルスがアカントアメーバを含む多種の微生物を感染・溶解する能力を持つことは確認されており、海洋・淡水の微生物生態系に実質的な影響を与えている可能性がある。
アベルジェル博士は、パンドラウイルスの環境的役割についてこう述べている。「パンドラウイルスは、炭素と酸素の生産に関与している。2,000個以上の遺伝子を持っており、それがどんなタンパク質・酵素をコードしているかはまだわからない。この種のウイルスの深い研究は、バイオテクノロジーへの重要な影響を持つだけでなく、炭素循環に関する私たちの理解を深めることにもなる」
海洋環境でのパンドラウイルスの実際の分布については、まだ解明が進んでいない。発見者たちが指摘するように、「発見が遅れた理由のひとつは、堆積物環境で主に生息しており、それが十分に研究されてこなかったからだ」。海底堆積物は、地球で最も広大でありながら、最も探索が進んでいない環境のひとつだ。
2022年のクラブリー&アベルジェルらによる永久凍土研究では、パンドラウイルスのゲノム断片が古代の凍土のメタゲノム解析からも検出されたが、凍土内ではパンドラウイルスの比率は比較的低かったことが報告されている。一方、世界各地の海水・淡水・土壌のメタゲノム研究では、パンドラウイルス様の配列が地球規模で広く分布していることが示唆されている。
「私たちのもっとも新しい発見は、巨大ウイルスが地球上のあらゆる場所に存在することを示した。15,000km離れた二か所でパンドラウイルスを発見したことは、このウイルスの偏在性を示している」とアベルジェルは語っている。
現在、地球上で最も多くの遺伝情報を格納しているのは生物ではなくウイルスだと考えられている。海洋だけでも約10³¹個のウイルスが存在し、その遺伝的多様性は細菌・古細菌・真核生物の合計を上回ると推定されている。ネブラスカ大学のジェームズ・ヴァン・エッテン(James Van Etten)教授はこう述べる:「地球上で最大の遺伝子源はおそらくウイルスだ——それらはどこにでもいるが、一般的に自分が繁殖する生物に対して非常に特異的だ」。パンドラウイルスの「93%未知遺伝子」は、この巨大な未知の遺伝子バンクのほんの一端を垣間見せてくれたに過ぎない。地球の生命の本当の多様性は、私たちが教科書で学んだものの何倍もの大きさである可能性が高い。
生命とは何か
——パンドラが問う哲学
ウイルスは生きているのか?細胞を持たなければ生命ではないのか?2,556の遺伝子を持ち、宿主の核を書き換え、自分の「工場」を建設するパンドラウイルスは、「生命」という概念そのものへの問いかけだ。
科学の歴史において、「生命の定義」ほど繰り返し議論され、繰り返し書き換えられてきたテーマはない。
アリストテレスは「自ら動く能力」を生命の本質とした。デカルトは生命を精巧な機械とみなした。シュレーディンガーは1944年の著書『生命とは何か』で「生命は負のエントロピーを食べる」と論じた。20世紀後半の分子生物学の発展によって、「自己複製するDNA/RNAを持つ存在」が生命の核心とされるようになった。
現在の教科書的定義は概ね以下の通りだ:①細胞という区画化された構造を持つ、②代謝(エネルギー変換)を行う、③自己複製能力を持つ、④環境への応答・適応能力を持つ、⑤進化する。
この定義によれば、ウイルスは①と②を欠くため「生命ではない」となる。しかしパンドラウイルスはこの判定を笑い飛ばすかのように、定義の境界線を侵食し続けている。
パンドラウイルスと「生命の定義」5条件の照合
①細胞構造:持たない。ただし宿主の核膜を書き換え、「ウイルス工場」を作る。これを「仮設の細胞」と呼べるか?
②代謝:独立した代謝は行わない。しかし2,500超の遺伝子の多くが何らかの代謝的機能をコードしている可能性があり、宿主細胞内での「寄生的代謝」は非常に能動的だ。
③自己複製:宿主なしには複製できないが、宿主内では極めて能動的・指揮的に複製する。「完全な自律性がなければ自己複製ではない」とするか、「方向性を持った複製であれば自己複製だ」とするかで解釈が分かれる。
④環境応答・適応:ある。宿主のアカントアメーバが飢餓状態になると、感染様式を変える可能性が示唆されている(ミミウイルスで確認されている現象)。
⑤進化:している——しかもde novo遺伝子創造という、他のどの生物にも類を見ない方法で、能動的に。
結論:3/5の条件を満たし、残り2つも「満たさない」とは言い切れない。「生命か否か」の二値判定は、パンドラウイルスに対して機能しない。
この問いに対して、フランスの微生物学者パトリック・フォルテール(Patrick Forterre)は「ヴァイロセル(virocell)」という概念を提唱している。ウイルスが感染した細胞は、もはやその「宿主」ではなく、ウイルスと細胞が融合した新しい「実体(virocell)」として捉えるべきだという考え方だ。この観点に立てば、パンドラウイルスが感染したアカントアメーバは「アカントアメーバ+パンドラウイルス」の合体生物であり、そこにはれっきとした「生命の活動」が存在する。
また、ウイルスの「生命の樹」への組み込みを主張する研究者の一派は、ウイルスが単なる「遺伝子の箱」ではなく、地球の生命進化において能動的な役割を担ってきたことを強調する。現在ヒトゲノムの約8%がウイルス(特にレトロウイルス)に由来することが判明している。人類の「自己(self)」の8%は、かつてのウイルス感染の遺産なのだ。パンドラウイルスが、さらに深い時間スケールで生命の進化に関与してきた可能性を否定できない。
2001年、東京理科大学の武村政春教授が提唱した「細胞核ウイルス起源説」は、まさにこの発想を突き詰めている。大型DNAウイルスの祖先が古細菌に感染・共生し、その過程で核膜が形成されたという仮説だ。もしこれが正しければ、動物・植物・菌類を含むすべての真核生物の細胞核は——ウイルスが残していった「遺産」ということになる。地球上の複雑な生命は、ウイルスの寄与なしには誕生しなかったかもしれない。
「すべてのゲノムはウイルス配列を含んでいる——それは遺伝子調節にも不可欠な要素だ。ウイルスは単なる病原体ではなく、水圏と生物圏における重要なプレイヤーだ」
パンドラウイルスを取り巻く哲学的問いは、科学的問いと表裏一体だ。「生命とは何か」という問いは、「どこから来たのか(起源)」「どこへ向かうのか(進化)」という問いと不可分に結びついている。そしてパンドラウイルスは、その両方の問いに対して、今まで誰も想定しなかった「答えの可能性」を提示している。
パンドラウイルスの遺伝子の93%は未知だ。その謎が解かれる日、人類は「生命とは何か」についての認識を根本から更新しなければならないかもしれない。あるいは、パンドラウイルスの謎は永遠に解けないかもしれない——ちょうど、パンドラの箱が一度開かれたら元に戻せないように。
ギリシャ神話では、パンドラが箱(ピトス)を開けると、疫病・悲嘆・貧困・嫉妬・憎しみなどあらゆる災厄が飛び出し、世界に広まった。パンドラが慌てて蓋を閉めると、箱の底にただひとつ残ったものがあった。それが「エルピス(Elpis)」——「希望」だ。
パンドラウイルスという名も、この神話と深くリンクしている。発見者たちが開けた「箱」から飛び出したのは、確かに恐ろしい謎だった——生命の定義の崩壊、第四の生命ドメインの可能性、永久凍土に眠るゾンビウイルスの脅威。しかしその箱の底に残っているのは、希望ではないだろうか。地球上にはまだ私たちが読めない生命の章がある、という希望。未知の93%の遺伝子の中に、医薬品・バイオテク・生命の起源への手がかりが眠っている、という希望。「生命の限界」という言葉が意味を失う日が来るかもしれない、という希望。
箱はまだ
開き続けている
2013年の発見から10年以上が経った今も、パンドラウイルスの謎は解けていない。むしろ、調べれば調べるほど謎は深まる。地球の深海と凍土と堆積物の中に、まだ何が眠っているのか——誰も知らない。
2013年の発見以来、パンドラウイルス研究は着実に進んでいる。新種の発見が相次ぎ(2018年時点で6種、その後もさらに増加)、永久凍土からの復活が確認され、CRISPR/Cas9による遺伝子操作が可能になった。日本でも国産パンドラウイルスが分離され、牛久沼では別の新種巨大ウイルスが見つかった。
しかし根本的な謎は残る。
93%の遺伝子が何をしているのか、まだわからない。パンドラウイルスがどこから進化したのか、まだわからない。「第四のドメイン」があるのかどうか、まだわからない。地球の海洋・土壌・凍土にどれほどのパンドラウイルスが生息しているか、まだわからない。そして、パンドラウイルスの未知の遺伝子のどれかが、人類に有益なものをもたらすかもしれないが——それも、まだわからない。
アベルジェル博士の言葉が繰り返し思い起こされる。「私たちの微生物学の知識は表面を引っ搔いたに過ぎない。探索されていない環境の中に、まだ重要な手がかりが眠っているかもしれない」
「パンドラウイルスの発見は、地球上の微生物の多様性に関する私たちの知識がいかに表面的であるかを示している。基本的な生命の性質についての重要な手がかりが、まだ探索されていない環境の中に潜んでいるかもしれない」
現在、クラブリーとアベルジェルはエクス=マルセイユ大学のIGS研究室で研究を続けている。新型コロナウイルス感染症のパンデミックの最中にも、彼らは永久凍土のウイルスに関する研究を発表し、「気候変動が解き放つ古代の病原体」というテーマへの警告を続けた。
ジャン=ミシェル・クラブリーは、2022年のCNNのインタビューでこう語った。「私たちはこれらのアメーバを感染させるウイルスを、他のすべての可能性があるウイルスの代理指標として見ています。アカントアメーバ以外の宿主——脊椎動物を含む——を感染させるウイルスが同様の条件の中で同様の感染能力を維持しているという合理的な推論が成立します」
ウイルスの宇宙は、まだ広がり続けている。2003年のミミウイルス以来、巨大ウイルスの「宇宙」は急速に拡大してきた——ミミウイルス、メガウイルス、パンドラウイルス、ピトウイルス、モリウイルス、ツパンウイルス、メドゥーサウイルス、ウシクウイルス、そしてまだ名前を持たない数多くの「未知の怪物」たち。そのひとつひとつが、「ウイルスとは何か」「生命とは何か」という問いへの新しい回答を突きつけてくる。
パンドラの箱は、開いてしまった。その中から何が飛び出すか——科学者たちは今日も、電子顕微鏡の前に座って、そのひとつひとつと向き合っている。
そして箱の底には、まだ「エルピス(希望)」が残っている。
📚 出典・参考文献
doi: 10.1126/science.1239181
※パンドラウイルス発見の原著論文
doi: 10.1073/pnas.1320670111
※ピトウイルス・シベリクム(3万年前)発見論文
doi: 10.1038/s41467-018-04698-4
※パンドラウイルスde novo遺伝子創造の発見
Abergel, C., Legendre, M., & Claverie, J.-M. (2015). The rapidly expanding universe of giant viruses: Mimivirus, Pandoravirus, Pithovirus and Mollivirus. FEMS Microbiology Reviews, 39(6), 779–796.
doi: 10.1093/femsre/fuv037
doi: 10.1073/pnas.1510795112
※モリウイルス発見および永久凍土ウイルスの温暖化リスクに関する論文
doi: 10.3390/v15020564
※2022年:13種の新ウイルス(最古48,500年)をシベリア凍土から復活させた論文
doi: 10.1038/s41467-023-36145-4
※CRISPR/Cas9でパンドラウイルスの遺伝子操作に初成功
doi: 10.1016/j.tim.2014.07.004
※「第四のドメイン説」への反論論文
ISBN: 978-4-06-257902-2
※パンドラウイルスと第四のドメインについての日本語解説書
※細胞核ウイルス起源説と巨大ウイルスの進化論的役割
https://en.wikipedia.org/wiki/Pandoravirus
https://ja.wikipedia.org/wiki/パンドラウイルス属
doi: 10.1038/nature.2013.13410
https://www.nationalgeographic.com/science/article/130718-viruses-pandoraviruses-science-biology-evolution
https://www.nationalgeographic.com/culture/article/140303-giant-virus-permafrost-siberia-pithovirus-pandoravirus-science
https://www.france24.com/en/20130802-giant-virus-pandora-box-pandoravirus-france-aix-science
https://www.cnrs.fr/en/press/pandoravirus-giant-viruses-invent-their-own-genes
https://www.sciencedaily.com/releases/2018/06/180611133505.htm
https://www.cnn.com/2023/03/08/world/permafrost-virus-risk-climate-scn
https://www.tus.ac.jp/today/archive/20200909_2345.html
https://www.ims.riken.jp/poster_virus/eco/mimi/
https://www.nikkei-science.com/202207_030.html
https://wired.jp/article/ushikuvirus-giant-virus-discovery-japan/
https://www.weforum.org/stories/2017/05/the-deadly-diseases-being-released-by-climate-change/
https://natgeo.nikkeibp.co.jp/nng/article/news/14/8175/











コメント